衡陽市中心醫(yī)院
臨床試驗倫理委員會章程
第一章 總 則
第一條 為保護(hù)臨床研究受試者的權(quán)益和安全���,規(guī)范本倫理委員會的組織和運作����,根據(jù)國家藥品監(jiān)督管理局《藥物臨床試驗質(zhì)量管理規(guī)范》(2020年)��、《赫爾辛基宣言》����、國際醫(yī)學(xué)科學(xué)組織理事會《涉及人的生物醫(yī)學(xué)研究國際倫理準(zhǔn)則》�����、《臨床試驗倫理審查工作指導(dǎo)原則》(2010年)和《涉及人的生物醫(yī)學(xué)研究倫理審查辦法》(2016年)等法律���、法規(guī)和有關(guān)部門的要求制定本章程��。
第二條 衡陽市中心醫(yī)院臨床試驗倫理委員會的宗旨是通過對臨床研究項目的科學(xué)性���、倫理合理性進(jìn)行審查��,確保受試者尊嚴(yán)�、安全和權(quán)益得到保護(hù)��,促進(jìn)生物醫(yī)學(xué)研究達(dá)到科學(xué)和倫理的高標(biāo)準(zhǔn)�,增強(qiáng)公眾對臨床研究的信任和支持。
第二章 組織
第三條 本倫理委員會名稱:衡陽市中心醫(yī)院臨床試驗倫理委員會��。
第四條 地址:湖南省衡陽市雁峰區(qū)雁城路10號����。
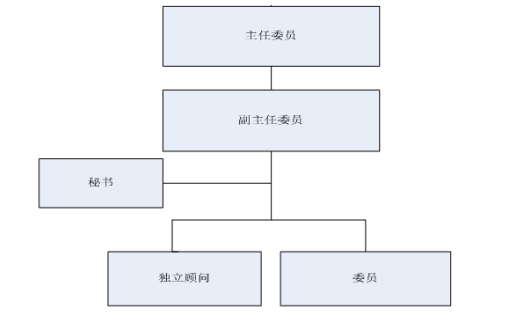
第五條 組織架構(gòu)圖如下:
第六條 職責(zé)
倫理委員會應(yīng)根據(jù)倫理審查工作的需要不斷完善組織管理和制度建設(shè),履行保護(hù)受試者的安全和權(quán)益的職責(zé)�。其職責(zé)的履行通過對申請人提交的藥物臨床試驗項目的倫理問題進(jìn)行獨立、公正�����、公平和及時審查來實現(xiàn)����。主要包括:初始審查��、跟蹤審查和快審���。
第七條 權(quán)力:
倫理委員會對藥物臨床試驗進(jìn)行審查監(jiān)督可以行使如下權(quán)力:
(一)批準(zhǔn)/不批準(zhǔn)一項藥物臨床試驗;
(二)對批準(zhǔn)的臨床試驗進(jìn)行跟蹤審查�����;
(三)終止或暫停已經(jīng)批準(zhǔn)的臨床試驗����。
第八條 行政資源:
倫理委員會的工作需要醫(yī)院的行政資源支持,包括:
(一) 獨立的行政匯報關(guān)系����,不受行政級別以及任何研究人員的影響開展獨立公正的倫理審核。獨立指獨立于所審查的項目�,與項目利益相關(guān)的倫理委員會人員應(yīng)避免利益沖突,醫(yī)院行政領(lǐng)導(dǎo)不得通過行政手段干預(yù)倫理委員會的工作���。
(二) 從行政上確保倫理委員成員有足夠的時間和精力參與倫理委員會工作。
(三) 倫理委員會的決議必須能貫徹實施���,研究人員不得違反倫理委員會規(guī)定開展相關(guān)臨床試驗工作�。
第九條 財政資源:
倫理委員會為非營利性機(jī)構(gòu),醫(yī)院在財政上提供相應(yīng)的資助���。財政來源可以是醫(yī)院的撥款已經(jīng)被審查項目提交的倫理審查費��。
倫理委員會的所有收入不得挪做他用�����,只能用于倫理委員會自身的建設(shè)發(fā)展(如委員的培訓(xùn)����、辦公條件的改善等)和必要的勞務(wù)開支����。
第三章 組建與換屆
第十條 首次組建倫理委員會成員由醫(yī)院院委會推薦,醫(yī)藥相關(guān)專業(yè)技術(shù)人員在醫(yī)院各專業(yè)專家中選取���,其它人員依據(jù)國家《臨床試驗質(zhì)量管理規(guī)范》和《臨床試驗倫理委員會工作指導(dǎo)原則》有關(guān)倫理委員會組成人員的規(guī)定,由醫(yī)院決定���,所有成員以醫(yī)院正式文件形式任命。
第十一條 倫理委員會設(shè)主任委員一名����,副主任委員一名����,由倫理委員會委員選舉產(chǎn)生��。
第十二條 倫理委員會設(shè)倫理秘書一名����,負(fù)責(zé)受理倫理審查項目、安排會議日程����、會議記錄、決議通告�����、檔案管理及其他日常工作����。
第十三條 倫理委員會根據(jù)所審查試驗項目的需要,可聘請獨立顧問�����,獨立顧問不參與投票����,僅對所審查項目發(fā)表專業(yè)意見。
第十四條 每屆倫理委員會組成人員不少于10人�,且性別均衡,任期五年�����,到期換屆�����,可連選連任�。換屆采取公開征集或由當(dāng)屆委員推薦備選人員,最終名單由當(dāng)屆倫理委員討論決定���,以會議紀(jì)要形式確定����,醫(yī)院正式文件任命����。
第十五條 倫理委員會主任委員可根據(jù)委員的工作表現(xiàn)及倫理委員會發(fā)展的需求�����,解聘或增補(bǔ)相關(guān)人員��,解聘或增補(bǔ)均需要超過全體委員的半數(shù)人員同意后方可正式解聘或聘任���。
第四章 工作程序
第十六條 倫理委員會應(yīng)本著獨立、公正���、科學(xué)的原則開展倫理審查工作�,不得受任何不利于受試者保護(hù)的因素影響���。倫理委員會應(yīng)遵循《藥物臨床試驗質(zhì)量管理規(guī)范》(GCP)和世界醫(yī)學(xué)會《赫爾辛基宣言》�����、國際醫(yī)學(xué)科學(xué)組織理事會《涉及人的生物醫(yī)學(xué)研究國際倫理準(zhǔn)則》等相關(guān)的國際倫理準(zhǔn)則����,在進(jìn)行臨床試驗倫理審查時���,要以確保受試者的權(quán)益��、安全和健康高于對科學(xué)和社會利益的需求為目標(biāo)��。
第十七條 倫理委員會全體成員必須遵守衡陽市中心醫(yī)院臨床試驗倫理委員會管理制度和工作流程��,認(rèn)真�����、自覺履行崗位職責(zé)����,積極參加倫理委員會安排的會議�����,不得無故缺席�、遲到、早退��。并同意公開其姓名��、職業(yè)和隸屬關(guān)系���,簽署有關(guān)審查項目�、受試者信息和相關(guān)事宜的保密協(xié)議,利益沖突聲明����。
第十八條 本院牽頭或參與的所有臨床試驗,須取得倫理委員會的會議審查同意并簽署批準(zhǔn)意見后方可實施���,已批準(zhǔn)通過后進(jìn)行方案修訂需根據(jù)修訂情況待倫理委員會會議審查或快速審查或備案完成后方可執(zhí)行修訂后的方案��。
第十九條 申請���、受理、評議����、審定、下達(dá)衡陽市中心醫(yī)院臨床試驗倫理委員會批復(fù)均應(yīng)遵循衡陽市中心醫(yī)院臨床試驗倫理委員會標(biāo)準(zhǔn)操作規(guī)程���,且需要履行書面手續(xù)�����。
第二十條 倫理委員會的審查形式有:會議審查和快速審查�。按審查內(nèi)容可分為:初始審查、復(fù)審審查��、跟蹤審查��、方案修訂審查�、安全性報告審查、方案偏離審查等�。
第二十一條 會議審查時,要求到會委員數(shù)應(yīng)不少于總委員人數(shù)的三分之二�,否則視為無效��。
第二十二條 審評過程要嚴(yán)格保密�,倫理委員會所有人員在受聘時均應(yīng)簽署保密協(xié)議。
第二十三條 會議審查后��,倫理委員會秘書及時整理會議記錄���,并根據(jù)會議記錄和審查意見形成書面?zhèn)惱韺彶橐庖?/span>/批件�����。
第二十四條 倫理委員會主任委員簽發(fā)倫理審查批件/意見����,加蓋倫理委員會公章。對于否定性的決議��,應(yīng)有明確的解釋���。
第二十五條 倫理委員會的審查意見有以下幾種:
(一) 同意�����;
(二) 作必要修改后同意����;
(三) 不同意�����;
(四) 終止或暫停已經(jīng)批準(zhǔn)的臨床試驗��。
第二十六條 倫理委員會主任委員主持倫理審查工作����,簽發(fā)倫理批件。主任委員不在時��,由副主任委員代行主任委員職權(quán)���。
第二十七條 倫理委員會成員應(yīng)積極參加倫理審查會議�����,認(rèn)真履行其職責(zé)�。每個委員每年參加的倫理審查會議次數(shù)若少于全年會議的1/3,視為自動放棄其委員資格����,第二年則不再聘其為倫理委員會委員。
第二十八條 委員會例會每半年一次�,遇重要事項由主任臨時召開。
第二十九條 倫理委員會應(yīng)根據(jù)衡陽市衛(wèi)健委的管理要求每年向市衛(wèi)健委報告上年度倫理審查工作情況��。
第三十條 倫理委員會成員不得向其所審查的臨床試驗的利益相關(guān)者索取現(xiàn)金���、有價證券和禮品等任何不正當(dāng)?shù)慕?jīng)濟(jì)利益。
第五章 附則
第三十一條 本章程的標(biāo)準(zhǔn)操作規(guī)程另行制定�。
第三十二條 本章程自2021年7月 27日起執(zhí)行。
第三十三條 本章程由衡陽市中心醫(yī)院臨床試驗倫理委員會負(fù)責(zé)解釋��。